线粒体脑肌病合并癫痫发作
线粒体脑肌病是由线粒体DNA或核DNA缺陷导致的多系统疾病病变侵犯骨骼肌为主者称为线粒体肌病伴有中枢神经系统症状者称线粒体脑肌病中枢神经系统的线粒体功能障碍可导致癫痫发作。常见的合并癫痫发作的线粒体脑肌病类型包括线粒体脑肌病伴高乳酸血症和卒中样发作(MELAS)和肌阵挛性癫痫伴不整红边纤维(MERRF)。MELAS大部分由线粒体DNAA3243G的点突变引起临床进程高度多样;MERRF多见于儿童主要由线粒体DNAA8344G点突变所致。线粒体脑肌病癫痫的发病机制主要与线粒体DNA突变有关导致线粒体蛋白合成受阻、ATP不足从而引发线粒体病。治疗方面线粒体功能异常导致的癫痫发作症状顽固药物选择有限目前尚无针对MELAS特异性治疗的抗癫痫药物应用研究。丙戊酸虽为广谱抗癫痫药物但可加重线粒体脑肌病患者的癫痫发作使用时需谨慎。左乙拉西坦、拉莫三嗪、托吡酯等新型抗癫痫药物对部分癫痫发作类型有效但应用时也需注意其可能的副作用。近几年L精氨酸治疗MELAS癫痫的研究为临床治疗带来了希望。总之对于线粒体脑肌病癫痫的治疗目前仍需进一步探索和研究。
相关推荐
-
妇科诊疗技术操作标准规范_20622084

 2025-11-29 999+
2025-11-29 999+ -
妇科诊疗常规(已审)_20625126

 2025-11-29 999+
2025-11-29 999+ -
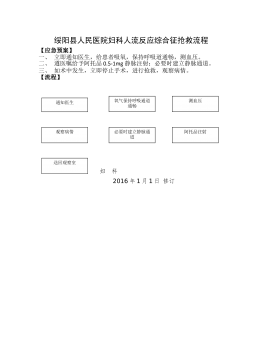
妇科人流综合症应急预案及流程_20622076
 2025-11-29 999+
2025-11-29 999+ -
妇科检查及二合诊三合诊图解_20622068

 2025-11-29 999+
2025-11-29 999+ -
妇科检查规范_20622067

 2025-11-29 999+
2025-11-29 999+ -
妇科护理常规讲解_20625121

 2025-11-29 999+
2025-11-29 999+ -
妇科护理常规_20622061

 2025-11-29 999+
2025-11-29 999+ -
妇科 不孕病(多囊卵巢综合征)中医临床路径_20625117

 2025-11-29 999+
2025-11-29 999+ -
二级病原微生物试验室生物安全管理规范-上海卫生和计划生育_20621748

 2025-11-29 999+
2025-11-29 999+ -
2022子宫内膜异位症【29页】

 2025-11-29 999+
2025-11-29 999+



