超声内窥镜标准草案
2025-10-14
999+
23.5KB
2 页
海报
侵权投诉
超声内窥镜(标准草案)
编制说明
一、工作简况
任务来源:本项目超声内镜(超声部分)由国家食品药品监督管理总局提出,根据《总局办公厅
关于印发2018年医疗器械行业标准制修订项目的通知》(食药监办械管〔2018〕**号),超声内镜
(超声部分)(项目计划号:A2018***-T-WH),由全国医用电器标准化技术委员会医用超声设备分技
术委员会(SAC/TC10/SC2)归口,制定工作由湖北省医疗器械质量监督检验研究院、深圳开立生物医疗
科技股份有限公司、北京华科创智健康科技股份有限公司、奥林巴斯(中国)有限公司完成。标准起
草人:轩辕凯、蒋时霖等。
二、标准编制原则和确定标准主要内容的依据
本标准依据GB/T 1.1-2009《标准化工作导则 第1部分 标准的结构和编写》给出的原则编制。
制定本标准的基本思路和方法是:针对在体(腔)内的使用环境,以科学、严密、实用、经济等为
原则,进行标准的编制。在现有环阵超声探头(使用试件),以及微凸阵超声探头(使用体模)测试
方法的基础上,推广到体(腔)内环型阵列和微凸阵阵列超声探头。
本标准主要依据医用超声诊断设备的一般性能及体(腔)内超声诊断设备的主要的独特的性能,确
定其标准的主要内容:
1、 声工作频率: 医用超声诊断设备一般应检测该指标,其要求与其他设备保持一致,即
“声工作频率与标称频率的偏差应在±15%范围之内。”;
2、 “探测深度”、“侧向分辨力”、“轴向分辨力”几项指标属于超声影像类设备应有的
常规指标,这些指标可以反映图像的清晰度,制造商应该公布,指标的限值由制造商决
定;
3、 “纵向几何位置精度”、“横向几何位置精度”依据相关制造商的建议确定了数值;
4、 “盲区”、“切片厚度”、“周长和面积测量偏差”、“M模式性能指标”、“三维成
像性能”等指标也属于超声影像类设备应有的常规指标,均未规定其指标限值,其限值
由制造商规定;
5、 “超声图像几何畸变”、“回撤方向几何位置精度”、“超声视野角”是“超声内镜”
的特殊要求;由于“超声内镜”探头的特殊性,以上指标需有适用制造商探头的体模或
试件来测试,本标准未规定体模或试件的型号,体模或试件只需满足试验要求即可。当
然如有不同于采用体模或试件的方法,然而该方法又可以验证本标准中的技术要求,也
可以采用;
6、 “外观和结构要求”和“使用功能要求”是一般产品标准应具备的要求;“电源电压适
应范围”和“连续工作时间”一般是针对90年代之前的产品的要求,随着科学的发展,
这两项指标对绝大多数厂家已不成问题,没有必要出现在本标准中。
7、 由于超声性能是整个超声内窥镜的一部分,本标准未规定环境试验的总体要求,只规定
了环境试验时应检测的项目,除按GB/T 14710《医用电器设备环境要求及试验方法》的
规定外,还可以按YY/T 1420《医用超声设备环境要求及试验方法》的原则和规定的内容
执行,适当放宽。
三、主要实验(或验证)的分析、综述报告、技术经济论证、预期经济效果
摘要:
展开>>
收起<<
《超声内窥镜(标准草案)》编制说明概要:本项目超声内镜(超声部分)标准由国家食品药品监督管理总局提出全国医用电器标准化技术委员会医用超声设备分技术委员会归口制定工作由湖北省医疗器械质量监督检验研究院等公司共同完成标准起草人为轩辕凯、蒋时霖等。标准依据标准化工作导则编制针对体腔内使用环境以科学、严密、实用、经济为原则推广现有探头测试方法到体腔内。标准主要内容涵盖声工作频率、探测深度等常规及特殊指标其中部分指标限值由制造商决定特殊指标需用适用体模或试件测试。同时本标准未规定环境试验总体要求只明确了应检测项目。本标准未采用国际标准未发现与现行法律、法规和其他强制性国际标准冲突。建议该标准作为推荐性行业标准发布后将开展宣贯工作。
相关推荐
-
妇科诊疗技术操作标准规范_20622084

 2025-11-29 999+
2025-11-29 999+ -
妇科诊疗常规(已审)_20625126

 2025-11-29 999+
2025-11-29 999+ -
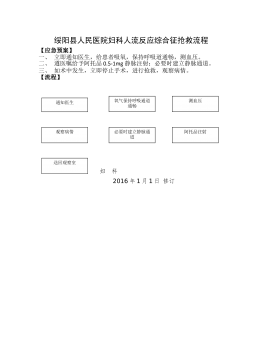
妇科人流综合症应急预案及流程_20622076
 2025-11-29 999+
2025-11-29 999+ -
妇科检查及二合诊三合诊图解_20622068

 2025-11-29 999+
2025-11-29 999+ -
妇科检查规范_20622067

 2025-11-29 999+
2025-11-29 999+ -
妇科护理常规讲解_20625121

 2025-11-29 999+
2025-11-29 999+ -
妇科护理常规_20622061

 2025-11-29 999+
2025-11-29 999+ -
妇科 不孕病(多囊卵巢综合征)中医临床路径_20625117

 2025-11-29 999+
2025-11-29 999+ -
二级病原微生物试验室生物安全管理规范-上海卫生和计划生育_20621748

 2025-11-29 999+
2025-11-29 999+ -
2022子宫内膜异位症【29页】

 2025-11-29 999+
2025-11-29 999+



