药品召回管理制度_33
2025-10-21
999+
13KB
2 页
海报
侵权投诉
药品召回管理制度
1、药品召回,是指按照规定的程序收回已上市销售的存在安全
隐患的药品。安全隐患,是指由于研发、生产等原因可能使药品具有
的危及人体健康和生命安全的不合理危险。
2、药剂科负责药品召回的管理。完善药品不良发应(ADR)报
告制度及相关制度,建立以质量管理部为中心,各相关部门为网络单
元的药品信息反馈、传递、分析及处理的完善的药品质量安全信息体
系。
(1)建立药品质量安全信息反馈记录,将信息及时反馈给有关
部门。
(2)建立和保存完整的购销记录,保证销售花纹路的可溯源性。
(3)质量管理部门配备专人负责药品质量安全信息收集、汇总
和处理,并负责对药品质量安全信息的处理进行归类存档。
(4)发现存在安全隐患的药品,应立即停止销售该药品,通知
药品生产企业和使用单位,并通知使用单位召回售出药品,并向药品
监督管理部门报告。
3、药品安全隐患的调查与评估:
(1)公司有责任和义务配合药品生产企业或者药品监督管理部
门开展有关药品安全隐患的调查,提供有关资料。
(2)药品安全隐患调查的内容应当根据实际情况确定,可以包
括:
A、已发生药品不良事件的种类、范围及原因。
B、药品使用是否符合药品说明书、标签规定的适应症、用法用
量的要求。
C、药品储存、运输是否符合要求。
D、可能存在安全隐患的药品批次、数量及流通区域和范围。
E、其化可能影响药品安全的因素。
(3)药品安全隐患评估的主要内容包括:
A、该药品引发危害的可能性,以及是否已经对人体健康造成了
摘要:
展开>>
收起<<
药品召回管理制度旨在收回存在安全隐患的已上市药品。安全隐患指因研发、生产等原因可能导致的危及人体健康和生命安全的危险。药剂科负责药品召回管理建立药品质量安全信息体系包括信息反馈记录、购销记录等并配备专人负责信息收集、汇总、处理及存档。发现安全隐患药品应立即停止销售通知生产企业和使用单位召回并向药监部门报告。公司需配合调查提供资料调查内容包括药品不良事件、使用情况、储存运输条件等。评估内容包括药品引发危害的可能性、对主要及特殊人群的影响、危害严重与紧急程度等。召回药品包括有效期内质量不稳定、包装标签说明书不符规定、确认存在严重安全隐患及药监部门强制召回的药品。医院作出召回决定后应立即通知相关单位并报告启动召回后需在规定时间内完成对召回药品处理应有详细记录并在药监部门监督下销毁需销毁药品召回完成后应对效果进行评价。
相关推荐
-
妇科诊疗技术操作标准规范_20622084

 2025-11-29 999+
2025-11-29 999+ -
妇科诊疗常规(已审)_20625126

 2025-11-29 999+
2025-11-29 999+ -
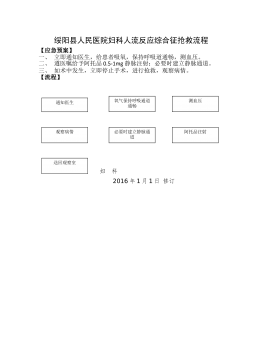
妇科人流综合症应急预案及流程_20622076
 2025-11-29 999+
2025-11-29 999+ -
妇科检查及二合诊三合诊图解_20622068

 2025-11-29 999+
2025-11-29 999+ -
妇科检查规范_20622067

 2025-11-29 999+
2025-11-29 999+ -
妇科护理常规讲解_20625121

 2025-11-29 999+
2025-11-29 999+ -
妇科护理常规_20622061

 2025-11-29 999+
2025-11-29 999+ -
妇科 不孕病(多囊卵巢综合征)中医临床路径_20625117

 2025-11-29 999+
2025-11-29 999+ -
二级病原微生物试验室生物安全管理规范-上海卫生和计划生育_20621748

 2025-11-29 999+
2025-11-29 999+ -
2022子宫内膜异位症【29页】

 2025-11-29 999+
2025-11-29 999+



