药物安全药理学研究技术指导原则
《附件1药物安全药理学研究技术指导原则》摘要安全药理学旨在研究药物在治疗范围内或以上剂量时对生理功能可能产生的不良影响特别是对中枢神经系统、心血管系统和呼吸系统的影响。必要时需进行追加和补充研究:前者指在怀疑已有试验结果可能影响人的安全性时对上述三系统进行深入研究;后者指评价药物对其他器官功能的影响如泌尿系统、自主神经系统等。其研究目的包括确定药物可能产生的非期望药理作用、评价药物在毒理学和临床研究中的不良反应等。研究应遵循以下原则:一是试验方法需根据药物特点和临床使用目的合理设计采用体内或体外方法;二是研究贯穿新药研究全过程临床试验前需完成核心组合试验;三是药物安全性评价研究须执行GLP规范核心组合试验必须执行GLP追加和补充研究应尽可能遵循;四是明确中药、天然药物及化学药物的受试物要求研发过程中受试物工艺变化若影响安全性则需进行相应研究。研究内容包括试验设计基本要求及主要研究内容。前者包括生物材料选择、样本量设定、剂量设计、对照设置、给药途径及次数选择、观察时间确定等;后者涵盖核心组合试验(研究药物对中枢神经系统、心血管系统、呼吸系统的影响)及追加和补充的安全药理学试验(针对潜在不
相关推荐
-
妇科诊疗技术操作标准规范_20622084

 2025-11-29 999+
2025-11-29 999+ -
妇科诊疗常规(已审)_20625126

 2025-11-29 999+
2025-11-29 999+ -
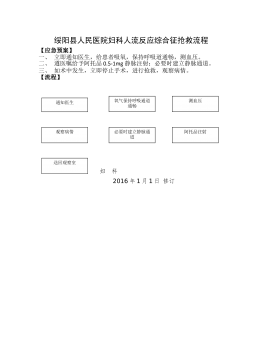
妇科人流综合症应急预案及流程_20622076
 2025-11-29 999+
2025-11-29 999+ -
妇科检查及二合诊三合诊图解_20622068

 2025-11-29 999+
2025-11-29 999+ -
妇科检查规范_20622067

 2025-11-29 999+
2025-11-29 999+ -
妇科护理常规讲解_20625121

 2025-11-29 999+
2025-11-29 999+ -
妇科护理常规_20622061

 2025-11-29 999+
2025-11-29 999+ -
妇科 不孕病(多囊卵巢综合征)中医临床路径_20625117

 2025-11-29 999+
2025-11-29 999+ -
二级病原微生物试验室生物安全管理规范-上海卫生和计划生育_20621748

 2025-11-29 999+
2025-11-29 999+ -
2022子宫内膜异位症【29页】

 2025-11-29 999+
2025-11-29 999+



